Гидроксисоединения относятся к категории органических веществ. Их молекулы содержат углеводородную цепь, а также функциональную группу ОН. Гидроксисоединения делятся на фенолы и спирты. Эти органические вещества получили большой спрос в различных отраслях. По характеру радикала спирты делятся на насыщенные и ненасыщенные. Если гидроксогруппа ОН соединена с бензольным кольцом, то такое вещество будет относиться к фенолам.
Краткое описание
Существует большое количество методов, с помощью которых можно получить спирт. Все доступные способы можно разделить на две категории:
- Биохимический. Спирт получают из природного растительного сырья.
- Химический. В лабораторных условиях при помощи специальных элементов получают спирт.
Оба способа изучают на уроках химии. Классификация спиртов зависит от присутствующего в составе углеводородного радикала. По этой причине выделяют предельную, непредельную, а также ароматическую группу, каждая из которых обладает определёнными характеристиками.
Для получения спиртов из карбонильных соединений применяется реакция восстановления. В этом случае используется каталитическое гидрирование. Восстановление возможно и в том случае, если различные доноры гидрид анионов будут действовать на кетоны и альдегиды. При последнем гидролизе образуется качественное органическое вещество.
Многоатомные спирты можно получить несколькими химическими способами:
- Мягкое окисление алкенов (гидроксилирование по Вагнеру).
- Щелочной гидролиз. В этом случае происходит нуклеофильное замещение атомов галогена на гидроксильные группы.
- Раскрытие эпоксидных циклов водой.
- Восстановление карбонильных соединений, которые содержат в своём составе функциональную гидроксильную группу.
Многоатомные органические соединения
Многоатомные спирты вступают в реакцию со щелочами, щёлочноземельными металлами, а также алюминием (должен быть заранее очищен от защитного покрытия Al2O3). Для замещения может использоваться любое количество атомов водорода.
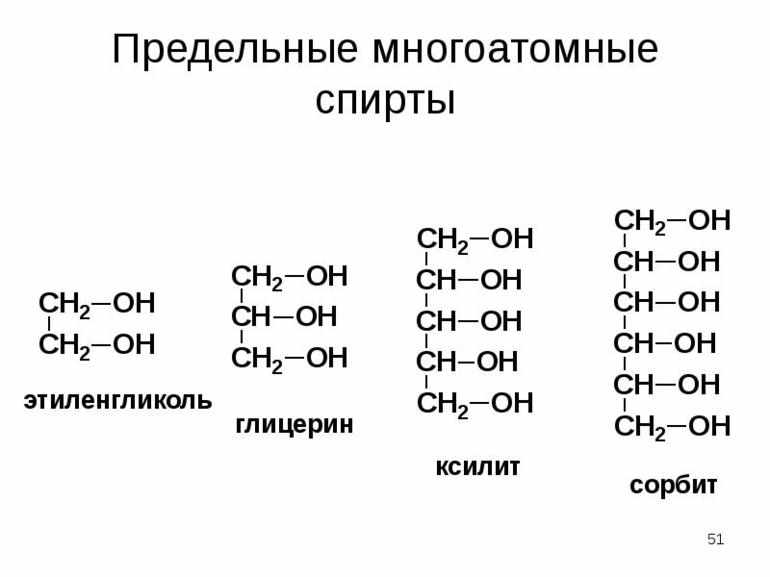
Молекулы многоатомных спиртов воздействуют друг на друга благодаря отрицательному индуктивному эффекту. В результате связь О-Н становится менее выраженной, а вот кислотные свойства гидроксильных групп стремительно возрастают. Высокая кислотность многоатомных спиртов заметна в том случае, когда они взаимодействуют с гидроксидами тяжёлых металлов.
Для лучшего усвоения правила следует рассмотреть пример. Свежеосажденный гидроксид меди реагирует на многоатомные спирты с последующим образованием раствора комплексного соединения. Жидкость будет окрашена в синий цвет. Эта реакция является качественной по отношению к многоатомным спиртам.
Физические свойства, токсичность С6Н5ОН
В нормальных условиях многие одноатомные фенолы представляют собой бесцветные кристаллические вещества, которые обладают характерным запахом. Для С6Н5ОН свойственна невысокая температура плавления. Фенолы практически не растворяются в воде, чего нельзя сказать об органических растворителях. С6Н5ОН — токсичное химическое вещество, которое в условиях хранения на открытом воздухе постепенно темнеет в результате окисления.
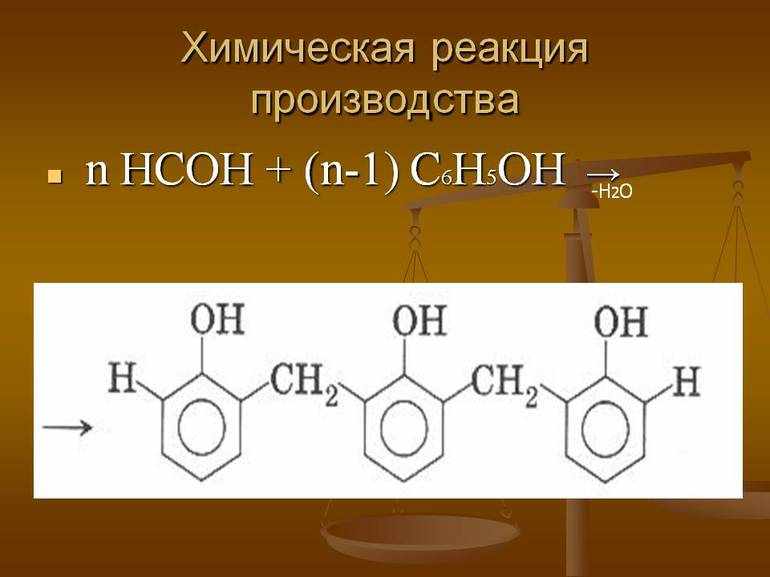
Фенол является бесцветным кристаллическим веществом. Под воздействием кислорода С6Н5ОН окисляется и приобретает розовый оттенок. Если нагреть фенол до отметки +60 °C или больше, тогда он смешается с водой в любом соотношении.
С6Н5ОН — токсичное вещество, которое вызывает ожоги кожи, а также серьёзные нарушения функций нервной системы. Раствор, пыль, а также пары фенола раздражают слизистые оболочки зрительного аппарата, дыхательных путей и кожного покрова. При попадании в организм С6Н5ОН быстро проникает в кровоток, из-за чего через 5−10 минут начинает воздействовать на ткани головного мозга, вызывая тем самым паралич дыхательного центра.