Специфичность химических свойств альдегидов обусловлена входящей в состав вещества альдегидной группы (карбонильной группы С=О, соединенной с атомом водорода). Выделяют 6 реакций: присоединительные (в т. ч. восстановления), полимеризации, окисления, замещения, поликонденсации и диспропорционирования. Взаимодействия, позволяющие определить наличие альдегида в составе смеси, носят название «качественные реакции».

Понятие альдегида
Альдегидом называют химическое вещество, в состав которого входит альдегидная группа и углеводородный радикал. Общую формулу предельного альдегида кратко можно записать: C (n)H (2 n) O. Альдегидная группа всегда расположена при первом атоме углерода.
Повышенная полярность связи С=О обуславливает два свойства:
- высокую полярность связи углерода с водородом,
- дефицит электронной плотности атома С альдегидной группы.

Первым в ряду альдегидов расположен формальдегид. В нем роль углеводородного радикала отведена молекуле водорода. Формальдегид самый активный. Его физическое состояние в нормальных условиях газообразное.
Реакция замещения
Водород, связанный с а-атомом углерода, может замещаться галогенами. Процесс носит название а-галогенирование, а продукты замещения называются лакриматорами.
Реакция замещения иллюстрируется пробой Люголя. В перенасыщенном растворе йода выдает присутствие альдегида желтый осадок — йодоформ. Катализатором выступает щелочь.
Реакция поликонденсации
Во время поликонденсации образуются новые углеродные связи, что приводит к появлению высокомолекулярных соединений. Процесс сопряжен с высвобождением молекул воды, соляной кислоты или других веществ.
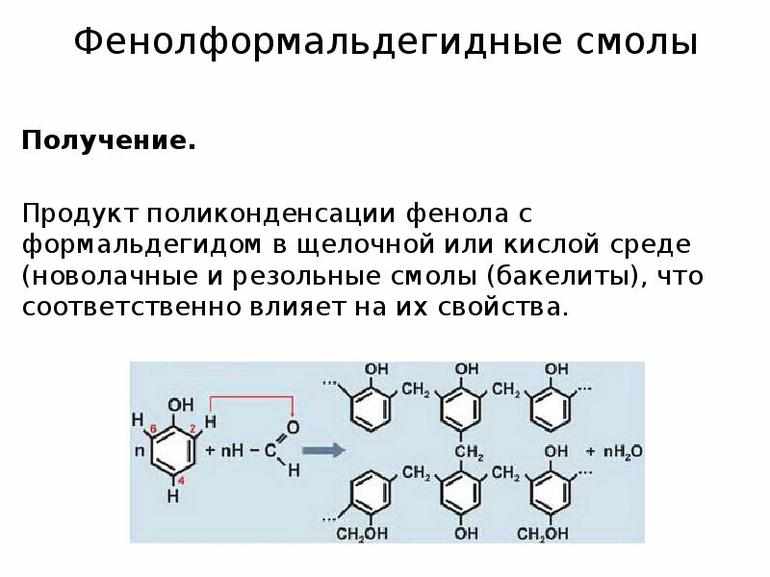
Фенолформальдегидные смолы образуются путем конденсации формальдегида с фенолом. Молекулы исходных веществ объединяются в фенолспирт. Катализатором выступает основание или кислота. Получившееся вещество вступает во взаимодействие с молекулами фенола. Поликонденсация сопровождается выделением воды. Сконденсированный продукт взаимодействует с формальдегидом. Следующий шаг — реакция с фенолом, потом с формальдегидом и так далее.
Процесс производства мочевиноформальдегидных смол основан на поликонденсации альдегидов с карбамидом, меламиноформальдегидных — с меламином.
Катализатором альдольной конденсации являются разбавленный раствор щелочи. Карбонильные группы двух молекул объединяются, образуя альдоль.
Нагрев альдегида или воздействие на него кислоты обуславливает кротоновую конденсацию (переход к непредельному альдегиду из предельного через альдоль). Процесс сопровождается выделением воды.
Реакция диспропорционирования
Встречается под названиями самоокисление-самовосстановление, или реакция Канниццаро. Условия протекания: воздействие щелочной среды на альдегид, а-углерод которого не связан с атомом водорода. Продукты диспропорционирования: спирт (восстановление), карбоновая кислота (окисление).
Применение альдегидов
Хим. свойства альдегидов нашли применение в промышленности. Присоединительные реакции взаимодействия со спиртом используют для получения ацеталей. Их запах можно описать как приятный, цветочный. Продукт взаимодействия бутиральдегида с поливиниловым спиртом используется при производстве безосколочных стекол (выполняет функцию клея). Продукты полимеризации используют для изготовления пленок, волокон. Метальдегид получил распространение в быту (более известен как «сухой спирт»).

В производстве зеркал, украшений, игрушек и т. п. используется реакция серебряного зеркала (окисление ацетальдегида аммиачным раствором оксида серебра). Выделяющийся в процессе реакции драгоценный металл осаждается на стенках сосуда, образуя декоративную зеркальную поверхность.
Лакриматоры (продукты реакции замещения) имеют слезоточивое действие. Часть из них (хлорацетофенон, бромацетон, хлорпикрин и другие) используют в полицейских и военных целях.
Фенолформальдегидные смолы нашли применение в производстве пластмасс. Меламиноформальдегидными смолами пропитывают материалы для придания им водостойкости и несминаемости. Альдольная конденсация используется для производства каучуков, смол, лаков и других веществ.