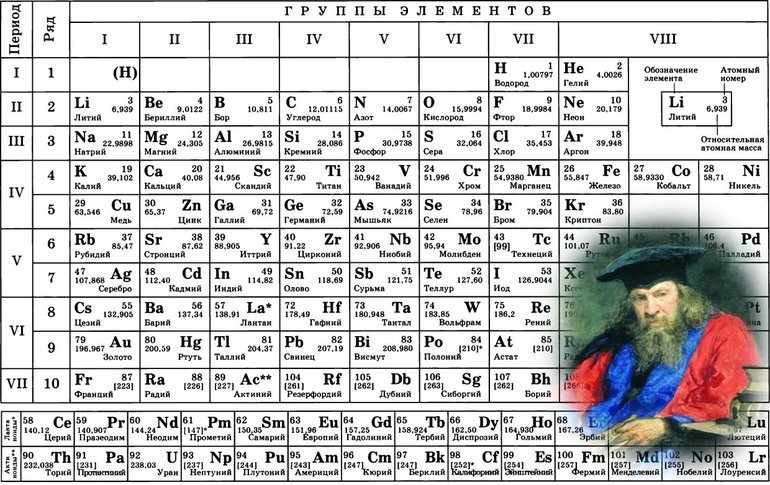
Сложные химические соединения состоят из различных элементов. В них электронная плотность всегда смещена в направлении более «сильного» соседа. Например, в атоме соляной кислоты таким окажется хлор. Чтобы определять силу атомов, необходимо разобраться с понятием электроотрицательности (ЭО). Эта величина обозначается буквой χ. Определяется электроотрицательность в таблице Менделеева.
Смысл понятия
Электроотрицательность химических элементов представляет собой способность атома вещества притягивать к себе электроны других атомов в сложных соединениях. Впервые это понятие ввел в начале XX столетия американский химик Лайнус Полинг. Простые элементы можно разделить на две большие группы в соответствии с их химическими и физическими свойствами:
- неметаллы,
- металлы.
Вещества из первой группы могут выступать в роли восстановителя либо окислителя в зависимости от показателя электроотрицательности элемента. Чем он выше, тем активнее вещество проявляет свойства окислителя.
Таким образом, необходимо разобраться с двумя новыми понятиями:
- Окислитель. Это реагент, который во время окислительно-восстановительной реакции принимает электроны.
- Восстановитель. Так называется вещество, которое может отдавать негативно заряженные частицы во время окислительно-восстановительной реакции.
Полингом была составлена специальная шкала электроотрицательности. Максимальной электронегативностию обладает фтор — 4. Минимальный электроотрицательный показатель у франция, и он равен 0,7.
Кроме этого, определить показатель электронегативности любого элемента можно по таблице Менделеева. Для этого необходимо запомнить два правила:
- В периодах с ростом заряда ядра электроотрицательность увеличивается слева направо.
- В группе значение ЭО снижается сверху вниз.

Зная эти правила, можно достаточно просто в любом соединении найти более сильный элемент. Однако химическим элементам нельзя приписывать постоянный показатель ЭО. Эта способность веществ зависит от различных факторов, в том числе от степени окисления и валентности.
Для полного понимания темы предстоит разобраться и с этими понятиями. Степенью валентности называется условный заряд атомов вещества в сложном соединении, определенный на базе предположения, что ионные и ковалентно-полярные соединения состоят исключительно из ионов. Также следует обратить внимание на тот факт, что в соединении суммарная степень окисления атомов равна нулю.
Валентность любого химического элемента определяется числом электронов, принимающих участие в образование химической связи между веществами. В отличие от степени окисления, валентность не имеет знака и не может быть равна нулю. Понятие относительной электроотрицательности (ОЭО) в химии нельзя игнорировать.
Именно с его помощью можно быстрее разобраться с принципами образования химических связей между элементами.